“신종 코로나 진단시약 1개 긴급승인…7일부터 민간기관서 사용”
입력 2020.02.04 (14:16)
수정 2020.02.04 (14:50)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.

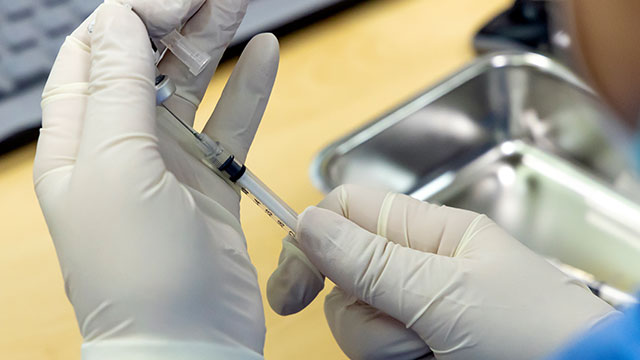
질병관리본부와 식품의약품안전처는 오늘(4일) 신종 코로나바이러스 진단시약 1개 제품에 대해 긴급사용을 승인했다고 밝혔습니다.
제품은 'PowerChekTM 2019-nCoV Real-time PCR Kit'이며 제조원은 ㈜코젠바이오텍입니다. 지난 2016년 메르스와 지카바이러스 진단시약에 이어 국내 두 번째 사례입니다.
식약처는 해당 업체의 신청자료와 성능시험, 전문가 검토 등을 통해 해당 제품의 진단정확성 등을 평가해 긴급사용을 승인했습니다.
승인제품은 질병관리본부가 지정한 민간의료기관에 공급돼 7일부터 환자 진단에 사용될 예정입니다.
보건당국 관계자는 "한시적으로 질병관리본부장이 인정하는 의료기관에서 신종 코로나바이러스 진단 검사가 가능하다"며 "의료기관은 7일 공개할 예정"이라고 설명했습니다.
'긴급사용 승인제도'는 감염병으로 긴급하게 진단시약이 필요하지만 국내에 허가제품이 없는 경우, 질병관리본부장이 요청한 진단시약을 식약처장이 승인해 한시적으로 제조·판매·사용할 수 있게 하는 제도입니다.
 ▶ ‘신종 코로나 바이러스 확산 우려’ 최신 기사 보기
▶ ‘신종 코로나 바이러스 확산 우려’ 최신 기사 보기http://news.kbs.co.kr/news/list.do?icd=19588
[사진 출처 : 연합뉴스]
제품은 'PowerChekTM 2019-nCoV Real-time PCR Kit'이며 제조원은 ㈜코젠바이오텍입니다. 지난 2016년 메르스와 지카바이러스 진단시약에 이어 국내 두 번째 사례입니다.
식약처는 해당 업체의 신청자료와 성능시험, 전문가 검토 등을 통해 해당 제품의 진단정확성 등을 평가해 긴급사용을 승인했습니다.
승인제품은 질병관리본부가 지정한 민간의료기관에 공급돼 7일부터 환자 진단에 사용될 예정입니다.
보건당국 관계자는 "한시적으로 질병관리본부장이 인정하는 의료기관에서 신종 코로나바이러스 진단 검사가 가능하다"며 "의료기관은 7일 공개할 예정"이라고 설명했습니다.
'긴급사용 승인제도'는 감염병으로 긴급하게 진단시약이 필요하지만 국내에 허가제품이 없는 경우, 질병관리본부장이 요청한 진단시약을 식약처장이 승인해 한시적으로 제조·판매·사용할 수 있게 하는 제도입니다.

[사진 출처 : 연합뉴스]
■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- “신종 코로나 진단시약 1개 긴급승인…7일부터 민간기관서 사용”
-
- 입력 2020-02-04 14:16:06
- 수정2020-02-04 14:50:50

질병관리본부와 식품의약품안전처는 오늘(4일) 신종 코로나바이러스 진단시약 1개 제품에 대해 긴급사용을 승인했다고 밝혔습니다.
제품은 'PowerChekTM 2019-nCoV Real-time PCR Kit'이며 제조원은 ㈜코젠바이오텍입니다. 지난 2016년 메르스와 지카바이러스 진단시약에 이어 국내 두 번째 사례입니다.
식약처는 해당 업체의 신청자료와 성능시험, 전문가 검토 등을 통해 해당 제품의 진단정확성 등을 평가해 긴급사용을 승인했습니다.
승인제품은 질병관리본부가 지정한 민간의료기관에 공급돼 7일부터 환자 진단에 사용될 예정입니다.
보건당국 관계자는 "한시적으로 질병관리본부장이 인정하는 의료기관에서 신종 코로나바이러스 진단 검사가 가능하다"며 "의료기관은 7일 공개할 예정"이라고 설명했습니다.
'긴급사용 승인제도'는 감염병으로 긴급하게 진단시약이 필요하지만 국내에 허가제품이 없는 경우, 질병관리본부장이 요청한 진단시약을 식약처장이 승인해 한시적으로 제조·판매·사용할 수 있게 하는 제도입니다.
 ▶ ‘신종 코로나 바이러스 확산 우려’ 최신 기사 보기
▶ ‘신종 코로나 바이러스 확산 우려’ 최신 기사 보기http://news.kbs.co.kr/news/list.do?icd=19588
[사진 출처 : 연합뉴스]
제품은 'PowerChekTM 2019-nCoV Real-time PCR Kit'이며 제조원은 ㈜코젠바이오텍입니다. 지난 2016년 메르스와 지카바이러스 진단시약에 이어 국내 두 번째 사례입니다.
식약처는 해당 업체의 신청자료와 성능시험, 전문가 검토 등을 통해 해당 제품의 진단정확성 등을 평가해 긴급사용을 승인했습니다.
승인제품은 질병관리본부가 지정한 민간의료기관에 공급돼 7일부터 환자 진단에 사용될 예정입니다.
보건당국 관계자는 "한시적으로 질병관리본부장이 인정하는 의료기관에서 신종 코로나바이러스 진단 검사가 가능하다"며 "의료기관은 7일 공개할 예정"이라고 설명했습니다.
'긴급사용 승인제도'는 감염병으로 긴급하게 진단시약이 필요하지만 국내에 허가제품이 없는 경우, 질병관리본부장이 요청한 진단시약을 식약처장이 승인해 한시적으로 제조·판매·사용할 수 있게 하는 제도입니다.
 ▶ ‘신종 코로나 바이러스 확산 우려’ 최신 기사 보기
▶ ‘신종 코로나 바이러스 확산 우려’ 최신 기사 보기[사진 출처 : 연합뉴스]
-
-

김민혁 기자 hyuk@kbs.co.kr
김민혁 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0
이슈
코로나19


















이 기사에 대한 의견을 남겨주세요.