식약처, ‘인보사’ 허가 취소·코오롱생명과학 형사 고발
입력 2019.05.28 (18:02)
수정 2019.05.28 (18:27)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.
[앵커]
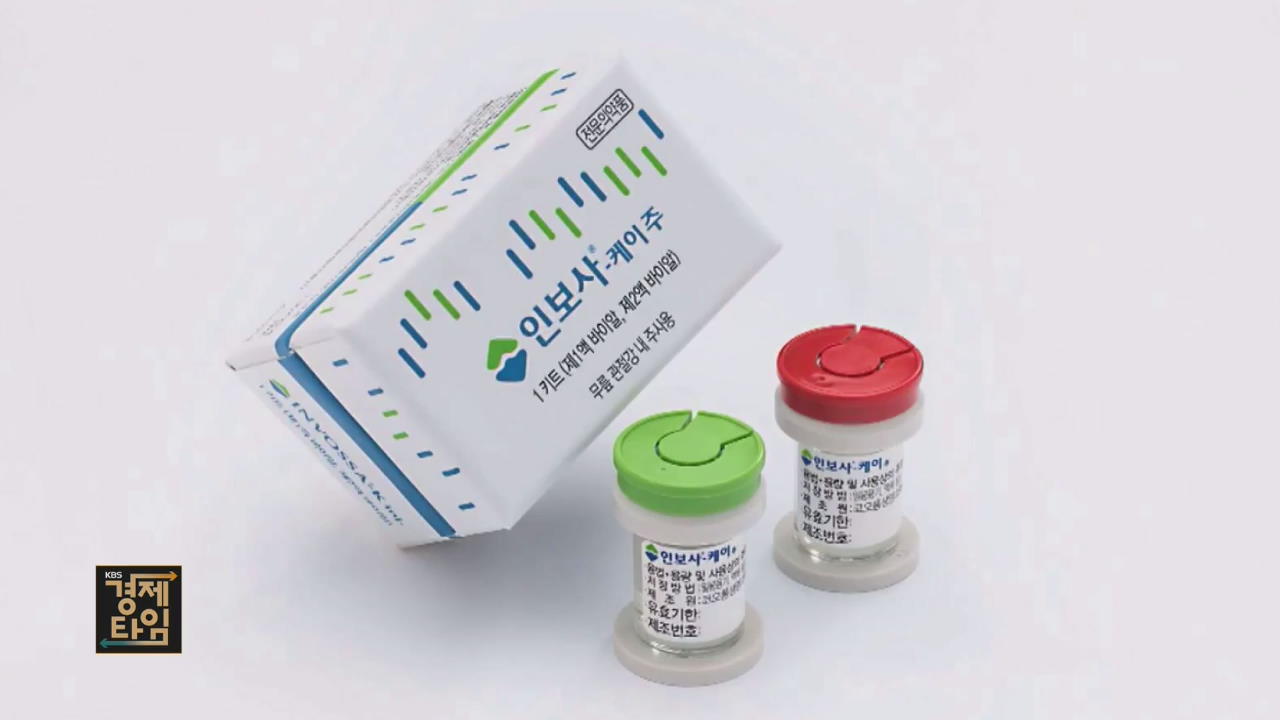
코오롱생명과학이 개발한 세계 최초 골관절염 유전자치료제, '인보사케이주'의 품목 허가가 취소됐습니다.
허가받지 않은 원료로 약물을 제조했다는 의혹이 사실로 확인됐기 때문인데, 식약처는 코오롱생명과학을 형사 고발하겠다고 밝혔습니다.
엄진아 기자가 보도합니다.
[리포트]
식품의약품안전처가 '인보사케이주'에 대한 품목 허가 취소를 공식 발표했습니다.
지난 2달간 코오롱생명과학에 대한 자료 분석과 美 현지 실사를 마친 결과, '인보사케이주'에 허가받지 않은 원료가 사용된 사실을 최종 확인됐다고 밝혔습니다.
주성분인 1액과 2액 가운데, 2액이 허가 당시 제출한 연골세포가 아닌 신장세포를 이용했다는 결론입니다.
제조사인 코오롱생명과학에 대해서는 형사 고발합니다.
식약처는 코오롱생명과학이 2017년 허가받기 이전에 일부 성분이 바뀐 것을 알았지만, 이를 숨기고 관련 자료를 제출하지 않았다고 판단했습니다.
심지어, 연골세포임을 증명하는 자료를 허위로 제출하고, 세포가 바뀐 이유에 대해 과학적 근거도 제시하지 못했다고 밝혔습니다.
허가 과정 등에 중대한 하자가 있었다는 것입니다.
인보사케이주는 2017년 7월 판매가 허용됐습니다.
무릎 통증에 획기적인 개선 효과를 기대하며 전국 430여 개 병의원에서 3,700여 명이 투약했습니다.
식약처는 부작용에 대비하기 위해 모든 환자에 대해 특별 관리하고, 앞으로 15년 동안 장기 추적 조사하겠다고 밝혔습니다.
한편, 인보사케이주를 투약한 환자 240여 명은 오늘, 코오롱생명과학에 대한 손해배상 청구소송을 제기합니다.
정신적 육체적 피해에 대한 제조사의 책임을 묻겠다는 의도입니다.
KBS 뉴스 엄진아입니다.
코오롱생명과학이 개발한 세계 최초 골관절염 유전자치료제, '인보사케이주'의 품목 허가가 취소됐습니다.
허가받지 않은 원료로 약물을 제조했다는 의혹이 사실로 확인됐기 때문인데, 식약처는 코오롱생명과학을 형사 고발하겠다고 밝혔습니다.
엄진아 기자가 보도합니다.
[리포트]
식품의약품안전처가 '인보사케이주'에 대한 품목 허가 취소를 공식 발표했습니다.
지난 2달간 코오롱생명과학에 대한 자료 분석과 美 현지 실사를 마친 결과, '인보사케이주'에 허가받지 않은 원료가 사용된 사실을 최종 확인됐다고 밝혔습니다.
주성분인 1액과 2액 가운데, 2액이 허가 당시 제출한 연골세포가 아닌 신장세포를 이용했다는 결론입니다.
제조사인 코오롱생명과학에 대해서는 형사 고발합니다.
식약처는 코오롱생명과학이 2017년 허가받기 이전에 일부 성분이 바뀐 것을 알았지만, 이를 숨기고 관련 자료를 제출하지 않았다고 판단했습니다.
심지어, 연골세포임을 증명하는 자료를 허위로 제출하고, 세포가 바뀐 이유에 대해 과학적 근거도 제시하지 못했다고 밝혔습니다.
허가 과정 등에 중대한 하자가 있었다는 것입니다.
인보사케이주는 2017년 7월 판매가 허용됐습니다.
무릎 통증에 획기적인 개선 효과를 기대하며 전국 430여 개 병의원에서 3,700여 명이 투약했습니다.
식약처는 부작용에 대비하기 위해 모든 환자에 대해 특별 관리하고, 앞으로 15년 동안 장기 추적 조사하겠다고 밝혔습니다.
한편, 인보사케이주를 투약한 환자 240여 명은 오늘, 코오롱생명과학에 대한 손해배상 청구소송을 제기합니다.
정신적 육체적 피해에 대한 제조사의 책임을 묻겠다는 의도입니다.
KBS 뉴스 엄진아입니다.
■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- 식약처, ‘인보사’ 허가 취소·코오롱생명과학 형사 고발
-
- 입력 2019-05-28 18:05:24
- 수정2019-05-28 18:27:06
[앵커]
코오롱생명과학이 개발한 세계 최초 골관절염 유전자치료제, '인보사케이주'의 품목 허가가 취소됐습니다.
허가받지 않은 원료로 약물을 제조했다는 의혹이 사실로 확인됐기 때문인데, 식약처는 코오롱생명과학을 형사 고발하겠다고 밝혔습니다.
엄진아 기자가 보도합니다.
[리포트]
식품의약품안전처가 '인보사케이주'에 대한 품목 허가 취소를 공식 발표했습니다.
지난 2달간 코오롱생명과학에 대한 자료 분석과 美 현지 실사를 마친 결과, '인보사케이주'에 허가받지 않은 원료가 사용된 사실을 최종 확인됐다고 밝혔습니다.
주성분인 1액과 2액 가운데, 2액이 허가 당시 제출한 연골세포가 아닌 신장세포를 이용했다는 결론입니다.
제조사인 코오롱생명과학에 대해서는 형사 고발합니다.
식약처는 코오롱생명과학이 2017년 허가받기 이전에 일부 성분이 바뀐 것을 알았지만, 이를 숨기고 관련 자료를 제출하지 않았다고 판단했습니다.
심지어, 연골세포임을 증명하는 자료를 허위로 제출하고, 세포가 바뀐 이유에 대해 과학적 근거도 제시하지 못했다고 밝혔습니다.
허가 과정 등에 중대한 하자가 있었다는 것입니다.
인보사케이주는 2017년 7월 판매가 허용됐습니다.
무릎 통증에 획기적인 개선 효과를 기대하며 전국 430여 개 병의원에서 3,700여 명이 투약했습니다.
식약처는 부작용에 대비하기 위해 모든 환자에 대해 특별 관리하고, 앞으로 15년 동안 장기 추적 조사하겠다고 밝혔습니다.
한편, 인보사케이주를 투약한 환자 240여 명은 오늘, 코오롱생명과학에 대한 손해배상 청구소송을 제기합니다.
정신적 육체적 피해에 대한 제조사의 책임을 묻겠다는 의도입니다.
KBS 뉴스 엄진아입니다.
코오롱생명과학이 개발한 세계 최초 골관절염 유전자치료제, '인보사케이주'의 품목 허가가 취소됐습니다.
허가받지 않은 원료로 약물을 제조했다는 의혹이 사실로 확인됐기 때문인데, 식약처는 코오롱생명과학을 형사 고발하겠다고 밝혔습니다.
엄진아 기자가 보도합니다.
[리포트]
식품의약품안전처가 '인보사케이주'에 대한 품목 허가 취소를 공식 발표했습니다.
지난 2달간 코오롱생명과학에 대한 자료 분석과 美 현지 실사를 마친 결과, '인보사케이주'에 허가받지 않은 원료가 사용된 사실을 최종 확인됐다고 밝혔습니다.
주성분인 1액과 2액 가운데, 2액이 허가 당시 제출한 연골세포가 아닌 신장세포를 이용했다는 결론입니다.
제조사인 코오롱생명과학에 대해서는 형사 고발합니다.
식약처는 코오롱생명과학이 2017년 허가받기 이전에 일부 성분이 바뀐 것을 알았지만, 이를 숨기고 관련 자료를 제출하지 않았다고 판단했습니다.
심지어, 연골세포임을 증명하는 자료를 허위로 제출하고, 세포가 바뀐 이유에 대해 과학적 근거도 제시하지 못했다고 밝혔습니다.
허가 과정 등에 중대한 하자가 있었다는 것입니다.
인보사케이주는 2017년 7월 판매가 허용됐습니다.
무릎 통증에 획기적인 개선 효과를 기대하며 전국 430여 개 병의원에서 3,700여 명이 투약했습니다.
식약처는 부작용에 대비하기 위해 모든 환자에 대해 특별 관리하고, 앞으로 15년 동안 장기 추적 조사하겠다고 밝혔습니다.
한편, 인보사케이주를 투약한 환자 240여 명은 오늘, 코오롱생명과학에 대한 손해배상 청구소송을 제기합니다.
정신적 육체적 피해에 대한 제조사의 책임을 묻겠다는 의도입니다.
KBS 뉴스 엄진아입니다.
-
-

엄진아 기자 aza@kbs.co.kr
엄진아 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0













![[단독] 도이치 주포 “김건희, 내 덕에 떼돈 벌어…22억 원 주문”](/data/news/2025/07/03/20250703_KpuU43.png)
![[단독] “쪽지 얼핏 봤다, 안 받았다”더니…CCTV에선 문건 챙긴 이상민](/data/news/2025/07/03/20250703_Lv3LjI.png)


이 기사에 대한 의견을 남겨주세요.