코오롱, ‘인보사 실험’ 암 걸린 생쥐 숨겼다?
입력 2020.04.29 (10:41)
수정 2020.04.29 (13:11)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.
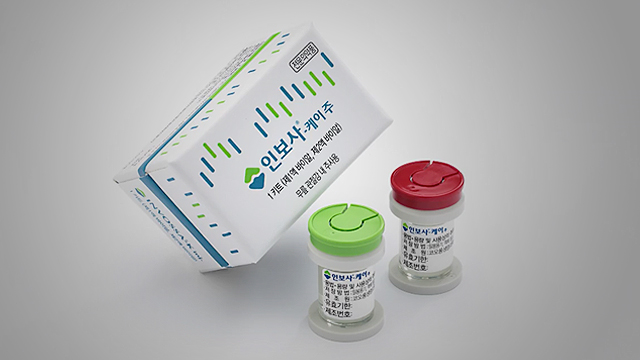
손상된 무릎연골을 재생시켜주는 '꿈의 치료제'로 각광받았던 인보사. 인보사 개발이 한창이던 2005년, 미국 코오롱티슈진은 생쥐에 인보사를 투여하는 실험을 합니다. 모든 세포치료제는 종양으로 발전할 위험을 내재하고 있는 만큼, 매우 중요한 실험이었습니다. 동물실험에서 안전성과 유효성이 확인되어야 사람을 대상으로 하는 임상시험으로 넘어갈 수 있기 때문입니다.
결과는 어땠을까요? 생쥐 10마리 중 3마리에게서 상피세포 악성종양, 즉 암이 발견됐습니다.
이후 미국 코오롱티슈진은 2006년 7월, 한국 코오롱생명과학은 2006년 12월 인보사 임상 승인을 받습니다. 그리고 11년 뒤인 2017년 마침내 식약처 허가를 받았습니다. '꿈의 치료제'가 완성된 겁니다. 하지만 지난해 3월 인보사 2액의 성분이 종양을 유발할 수 있는 신장유래세포인 것으로 드러나면서, 식약처는 허가를 취소하고 검찰에 코오롱생명과학을 고발했습니다. 검찰 수사 결과 식약처 고발 내용이 대부분 인정되면서 코오롱생명과학은 이우석 대표까지 구속기소 되는 수모를 겪었습니다.
■ 검찰 "암 걸린 생쥐, 왜 숨겼나?"
어제(27일)는 코오롱생명과학 관계자들의 2차 공판이 진행됐습니다. 이 재판에서 검찰이 중요하게 거론한 것 중 하나가 바로 서두에 언급한 2005년 동물실험입니다. 코오롱생명과학이 그동안 식약처에 제출한 자료 어디에도 종양이 발생한 동물실험을 보고한 사실을 찾을 수 없다는 겁니다.
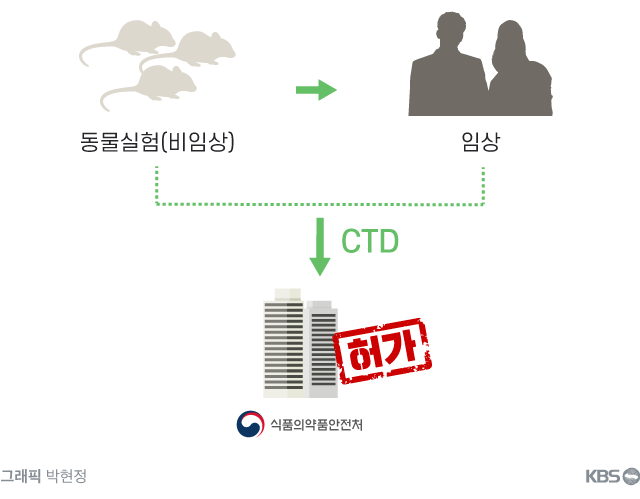
검찰은 오히려 코오롱생명과학이 '동물실험 결과 종양이 발견되지 않았다'는 허위 자료를 제출해 임상 승인을 받았다고 주장했습니다. 게다가 임상을 모두 마치고 의약품 허가를 받기 위해 최종적으로 식약처에 제출한 CTD(Common Technical Document)라는 서류 본문 어디에도 생쥐 10마리 중 3마리에서 악성종양이 발생한 실험 내용을 기재하지 않았다고 주장했습니다.
■ "알았다면 당연히 임상승인 안 됐겠죠"
증인으로 나온 식약처 정 모 과장은 만약 동물실험에서 종양이 발견된 사실을 알았다면, 인보사 허가는 어려웠을 것 같다고 증언했습니다. '종양이 발견되지 않았다'는 지금까지의 대전제 자체가 깨지기 때문에, 이를 해결하기 전까지는 임상 승인도 나지 않았을 거라는 겁니다. 정 과장은 종양이 발견됐든 발견되지 않았든 진행된 동물실험 결과는 모두 식약처에 보고해야 한다고 주장했습니다.
■ "식약처는 1,000장만 제대로 읽고 59,000장은 꼼꼼히 안 본단 말인가요?"
변호인은 뭐라고 반박했을까요? 먼저, 해당 실험을 식약처에 보고하지 않았다는 건 사실이 아니라고 밝혔습니다. CTD 본문 뒤에 붙어있는 '첨부자료'에 악성종양이 발견된 동물실험 결과가 언급돼 있다는 겁니다. 이에 대해 식약처 과장은 "현실적으로 첨부자료까지 다 검토하긴 어렵다"고 증언했습니다.
변호인은 인보사 CTD 서류 전체가 총 6만 장이라면서, 이 중 본문은 1,000장에 불과하고 나머지 59,000장은 첨부자료라고 설명했습니다. 그러면서 오히려 첨부자료를 제대로 확인하지 않은 식약처가 꼼꼼하지 못했던 것이 아니냐며 날을 세웠습니다. 국민 건강과 직결되는 의약품을 심사하는 식약처라면, 1,000장의 본문만 보고 의약품 허가를 결정할 게 아니라 첨부자료까지 모두 자세히 들여다봤어야 한다는 겁니다.
■ "식약처가 꼼꼼하지 않아서가 아니고요!"
식약처 과장도 바로 반박에 나섰습니다. 코오롱생명과학이 엉뚱한 곳에서 해당 실험을 언급했다는 겁니다. 제대로 기재하려면 CTD '종양 가능성' 부분에 이 실험 내용이 들어갔어야 하는데, 종양과는 아무 상관 없는 부분의 첨부자료에 해당 실험이 껴들어 갔다는 설명입니다. 검찰도 코오롱생명과학이 CTD 첨부자료에 간단한 표 형태로만 해당 실험을 언급했을 뿐, 자세한 연구보고서는 전혀 제출하지 않았다고 반박했습니다.
■ 미국 임상 재개, 코오롱생명과학의 '반전 드라마'?
지난 12일 미국 식품의약국(FDA)은 그동안 중단됐던 인보사 미국제품 임상3상을 재개한다는 결정을 내렸습니다. 국내제품 허가가 취소된 이후 절체절명의 위기를 맞이한 코오롱생명과학도 반전을 꿈꾸고 있는 것으로 보입니다. 하지만 식약처는 "미국 임상 재개는 국내 제품 허가 취소와 아무 상관 없다"고 단언하고 있습니다. 코오롱생명과학이 꿈꾸는 반전은 진짜 반전으로 이어질 수 있을까요?
결과는 어땠을까요? 생쥐 10마리 중 3마리에게서 상피세포 악성종양, 즉 암이 발견됐습니다.
이후 미국 코오롱티슈진은 2006년 7월, 한국 코오롱생명과학은 2006년 12월 인보사 임상 승인을 받습니다. 그리고 11년 뒤인 2017년 마침내 식약처 허가를 받았습니다. '꿈의 치료제'가 완성된 겁니다. 하지만 지난해 3월 인보사 2액의 성분이 종양을 유발할 수 있는 신장유래세포인 것으로 드러나면서, 식약처는 허가를 취소하고 검찰에 코오롱생명과학을 고발했습니다. 검찰 수사 결과 식약처 고발 내용이 대부분 인정되면서 코오롱생명과학은 이우석 대표까지 구속기소 되는 수모를 겪었습니다.
■ 검찰 "암 걸린 생쥐, 왜 숨겼나?"
어제(27일)는 코오롱생명과학 관계자들의 2차 공판이 진행됐습니다. 이 재판에서 검찰이 중요하게 거론한 것 중 하나가 바로 서두에 언급한 2005년 동물실험입니다. 코오롱생명과학이 그동안 식약처에 제출한 자료 어디에도 종양이 발생한 동물실험을 보고한 사실을 찾을 수 없다는 겁니다.
검찰은 오히려 코오롱생명과학이 '동물실험 결과 종양이 발견되지 않았다'는 허위 자료를 제출해 임상 승인을 받았다고 주장했습니다. 게다가 임상을 모두 마치고 의약품 허가를 받기 위해 최종적으로 식약처에 제출한 CTD(Common Technical Document)라는 서류 본문 어디에도 생쥐 10마리 중 3마리에서 악성종양이 발생한 실험 내용을 기재하지 않았다고 주장했습니다.

■ "알았다면 당연히 임상승인 안 됐겠죠"
증인으로 나온 식약처 정 모 과장은 만약 동물실험에서 종양이 발견된 사실을 알았다면, 인보사 허가는 어려웠을 것 같다고 증언했습니다. '종양이 발견되지 않았다'는 지금까지의 대전제 자체가 깨지기 때문에, 이를 해결하기 전까지는 임상 승인도 나지 않았을 거라는 겁니다. 정 과장은 종양이 발견됐든 발견되지 않았든 진행된 동물실험 결과는 모두 식약처에 보고해야 한다고 주장했습니다.
■ "식약처는 1,000장만 제대로 읽고 59,000장은 꼼꼼히 안 본단 말인가요?"
변호인은 뭐라고 반박했을까요? 먼저, 해당 실험을 식약처에 보고하지 않았다는 건 사실이 아니라고 밝혔습니다. CTD 본문 뒤에 붙어있는 '첨부자료'에 악성종양이 발견된 동물실험 결과가 언급돼 있다는 겁니다. 이에 대해 식약처 과장은 "현실적으로 첨부자료까지 다 검토하긴 어렵다"고 증언했습니다.
변호인은 인보사 CTD 서류 전체가 총 6만 장이라면서, 이 중 본문은 1,000장에 불과하고 나머지 59,000장은 첨부자료라고 설명했습니다. 그러면서 오히려 첨부자료를 제대로 확인하지 않은 식약처가 꼼꼼하지 못했던 것이 아니냐며 날을 세웠습니다. 국민 건강과 직결되는 의약품을 심사하는 식약처라면, 1,000장의 본문만 보고 의약품 허가를 결정할 게 아니라 첨부자료까지 모두 자세히 들여다봤어야 한다는 겁니다.
■ "식약처가 꼼꼼하지 않아서가 아니고요!"
식약처 과장도 바로 반박에 나섰습니다. 코오롱생명과학이 엉뚱한 곳에서 해당 실험을 언급했다는 겁니다. 제대로 기재하려면 CTD '종양 가능성' 부분에 이 실험 내용이 들어갔어야 하는데, 종양과는 아무 상관 없는 부분의 첨부자료에 해당 실험이 껴들어 갔다는 설명입니다. 검찰도 코오롱생명과학이 CTD 첨부자료에 간단한 표 형태로만 해당 실험을 언급했을 뿐, 자세한 연구보고서는 전혀 제출하지 않았다고 반박했습니다.
■ 미국 임상 재개, 코오롱생명과학의 '반전 드라마'?
지난 12일 미국 식품의약국(FDA)은 그동안 중단됐던 인보사 미국제품 임상3상을 재개한다는 결정을 내렸습니다. 국내제품 허가가 취소된 이후 절체절명의 위기를 맞이한 코오롱생명과학도 반전을 꿈꾸고 있는 것으로 보입니다. 하지만 식약처는 "미국 임상 재개는 국내 제품 허가 취소와 아무 상관 없다"고 단언하고 있습니다. 코오롱생명과학이 꿈꾸는 반전은 진짜 반전으로 이어질 수 있을까요?
■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- 코오롱, ‘인보사 실험’ 암 걸린 생쥐 숨겼다?
-
- 입력 2020-04-29 10:41:27
- 수정2020-04-29 13:11:46

손상된 무릎연골을 재생시켜주는 '꿈의 치료제'로 각광받았던 인보사. 인보사 개발이 한창이던 2005년, 미국 코오롱티슈진은 생쥐에 인보사를 투여하는 실험을 합니다. 모든 세포치료제는 종양으로 발전할 위험을 내재하고 있는 만큼, 매우 중요한 실험이었습니다. 동물실험에서 안전성과 유효성이 확인되어야 사람을 대상으로 하는 임상시험으로 넘어갈 수 있기 때문입니다.
결과는 어땠을까요? 생쥐 10마리 중 3마리에게서 상피세포 악성종양, 즉 암이 발견됐습니다.
이후 미국 코오롱티슈진은 2006년 7월, 한국 코오롱생명과학은 2006년 12월 인보사 임상 승인을 받습니다. 그리고 11년 뒤인 2017년 마침내 식약처 허가를 받았습니다. '꿈의 치료제'가 완성된 겁니다. 하지만 지난해 3월 인보사 2액의 성분이 종양을 유발할 수 있는 신장유래세포인 것으로 드러나면서, 식약처는 허가를 취소하고 검찰에 코오롱생명과학을 고발했습니다. 검찰 수사 결과 식약처 고발 내용이 대부분 인정되면서 코오롱생명과학은 이우석 대표까지 구속기소 되는 수모를 겪었습니다.
■ 검찰 "암 걸린 생쥐, 왜 숨겼나?"
어제(27일)는 코오롱생명과학 관계자들의 2차 공판이 진행됐습니다. 이 재판에서 검찰이 중요하게 거론한 것 중 하나가 바로 서두에 언급한 2005년 동물실험입니다. 코오롱생명과학이 그동안 식약처에 제출한 자료 어디에도 종양이 발생한 동물실험을 보고한 사실을 찾을 수 없다는 겁니다.
검찰은 오히려 코오롱생명과학이 '동물실험 결과 종양이 발견되지 않았다'는 허위 자료를 제출해 임상 승인을 받았다고 주장했습니다. 게다가 임상을 모두 마치고 의약품 허가를 받기 위해 최종적으로 식약처에 제출한 CTD(Common Technical Document)라는 서류 본문 어디에도 생쥐 10마리 중 3마리에서 악성종양이 발생한 실험 내용을 기재하지 않았다고 주장했습니다.

■ "알았다면 당연히 임상승인 안 됐겠죠"
증인으로 나온 식약처 정 모 과장은 만약 동물실험에서 종양이 발견된 사실을 알았다면, 인보사 허가는 어려웠을 것 같다고 증언했습니다. '종양이 발견되지 않았다'는 지금까지의 대전제 자체가 깨지기 때문에, 이를 해결하기 전까지는 임상 승인도 나지 않았을 거라는 겁니다. 정 과장은 종양이 발견됐든 발견되지 않았든 진행된 동물실험 결과는 모두 식약처에 보고해야 한다고 주장했습니다.
■ "식약처는 1,000장만 제대로 읽고 59,000장은 꼼꼼히 안 본단 말인가요?"
변호인은 뭐라고 반박했을까요? 먼저, 해당 실험을 식약처에 보고하지 않았다는 건 사실이 아니라고 밝혔습니다. CTD 본문 뒤에 붙어있는 '첨부자료'에 악성종양이 발견된 동물실험 결과가 언급돼 있다는 겁니다. 이에 대해 식약처 과장은 "현실적으로 첨부자료까지 다 검토하긴 어렵다"고 증언했습니다.
변호인은 인보사 CTD 서류 전체가 총 6만 장이라면서, 이 중 본문은 1,000장에 불과하고 나머지 59,000장은 첨부자료라고 설명했습니다. 그러면서 오히려 첨부자료를 제대로 확인하지 않은 식약처가 꼼꼼하지 못했던 것이 아니냐며 날을 세웠습니다. 국민 건강과 직결되는 의약품을 심사하는 식약처라면, 1,000장의 본문만 보고 의약품 허가를 결정할 게 아니라 첨부자료까지 모두 자세히 들여다봤어야 한다는 겁니다.
■ "식약처가 꼼꼼하지 않아서가 아니고요!"
식약처 과장도 바로 반박에 나섰습니다. 코오롱생명과학이 엉뚱한 곳에서 해당 실험을 언급했다는 겁니다. 제대로 기재하려면 CTD '종양 가능성' 부분에 이 실험 내용이 들어갔어야 하는데, 종양과는 아무 상관 없는 부분의 첨부자료에 해당 실험이 껴들어 갔다는 설명입니다. 검찰도 코오롱생명과학이 CTD 첨부자료에 간단한 표 형태로만 해당 실험을 언급했을 뿐, 자세한 연구보고서는 전혀 제출하지 않았다고 반박했습니다.
■ 미국 임상 재개, 코오롱생명과학의 '반전 드라마'?
지난 12일 미국 식품의약국(FDA)은 그동안 중단됐던 인보사 미국제품 임상3상을 재개한다는 결정을 내렸습니다. 국내제품 허가가 취소된 이후 절체절명의 위기를 맞이한 코오롱생명과학도 반전을 꿈꾸고 있는 것으로 보입니다. 하지만 식약처는 "미국 임상 재개는 국내 제품 허가 취소와 아무 상관 없다"고 단언하고 있습니다. 코오롱생명과학이 꿈꾸는 반전은 진짜 반전으로 이어질 수 있을까요?
결과는 어땠을까요? 생쥐 10마리 중 3마리에게서 상피세포 악성종양, 즉 암이 발견됐습니다.
이후 미국 코오롱티슈진은 2006년 7월, 한국 코오롱생명과학은 2006년 12월 인보사 임상 승인을 받습니다. 그리고 11년 뒤인 2017년 마침내 식약처 허가를 받았습니다. '꿈의 치료제'가 완성된 겁니다. 하지만 지난해 3월 인보사 2액의 성분이 종양을 유발할 수 있는 신장유래세포인 것으로 드러나면서, 식약처는 허가를 취소하고 검찰에 코오롱생명과학을 고발했습니다. 검찰 수사 결과 식약처 고발 내용이 대부분 인정되면서 코오롱생명과학은 이우석 대표까지 구속기소 되는 수모를 겪었습니다.
■ 검찰 "암 걸린 생쥐, 왜 숨겼나?"
어제(27일)는 코오롱생명과학 관계자들의 2차 공판이 진행됐습니다. 이 재판에서 검찰이 중요하게 거론한 것 중 하나가 바로 서두에 언급한 2005년 동물실험입니다. 코오롱생명과학이 그동안 식약처에 제출한 자료 어디에도 종양이 발생한 동물실험을 보고한 사실을 찾을 수 없다는 겁니다.
검찰은 오히려 코오롱생명과학이 '동물실험 결과 종양이 발견되지 않았다'는 허위 자료를 제출해 임상 승인을 받았다고 주장했습니다. 게다가 임상을 모두 마치고 의약품 허가를 받기 위해 최종적으로 식약처에 제출한 CTD(Common Technical Document)라는 서류 본문 어디에도 생쥐 10마리 중 3마리에서 악성종양이 발생한 실험 내용을 기재하지 않았다고 주장했습니다.

■ "알았다면 당연히 임상승인 안 됐겠죠"
증인으로 나온 식약처 정 모 과장은 만약 동물실험에서 종양이 발견된 사실을 알았다면, 인보사 허가는 어려웠을 것 같다고 증언했습니다. '종양이 발견되지 않았다'는 지금까지의 대전제 자체가 깨지기 때문에, 이를 해결하기 전까지는 임상 승인도 나지 않았을 거라는 겁니다. 정 과장은 종양이 발견됐든 발견되지 않았든 진행된 동물실험 결과는 모두 식약처에 보고해야 한다고 주장했습니다.
■ "식약처는 1,000장만 제대로 읽고 59,000장은 꼼꼼히 안 본단 말인가요?"
변호인은 뭐라고 반박했을까요? 먼저, 해당 실험을 식약처에 보고하지 않았다는 건 사실이 아니라고 밝혔습니다. CTD 본문 뒤에 붙어있는 '첨부자료'에 악성종양이 발견된 동물실험 결과가 언급돼 있다는 겁니다. 이에 대해 식약처 과장은 "현실적으로 첨부자료까지 다 검토하긴 어렵다"고 증언했습니다.
변호인은 인보사 CTD 서류 전체가 총 6만 장이라면서, 이 중 본문은 1,000장에 불과하고 나머지 59,000장은 첨부자료라고 설명했습니다. 그러면서 오히려 첨부자료를 제대로 확인하지 않은 식약처가 꼼꼼하지 못했던 것이 아니냐며 날을 세웠습니다. 국민 건강과 직결되는 의약품을 심사하는 식약처라면, 1,000장의 본문만 보고 의약품 허가를 결정할 게 아니라 첨부자료까지 모두 자세히 들여다봤어야 한다는 겁니다.
■ "식약처가 꼼꼼하지 않아서가 아니고요!"
식약처 과장도 바로 반박에 나섰습니다. 코오롱생명과학이 엉뚱한 곳에서 해당 실험을 언급했다는 겁니다. 제대로 기재하려면 CTD '종양 가능성' 부분에 이 실험 내용이 들어갔어야 하는데, 종양과는 아무 상관 없는 부분의 첨부자료에 해당 실험이 껴들어 갔다는 설명입니다. 검찰도 코오롱생명과학이 CTD 첨부자료에 간단한 표 형태로만 해당 실험을 언급했을 뿐, 자세한 연구보고서는 전혀 제출하지 않았다고 반박했습니다.
■ 미국 임상 재개, 코오롱생명과학의 '반전 드라마'?
지난 12일 미국 식품의약국(FDA)은 그동안 중단됐던 인보사 미국제품 임상3상을 재개한다는 결정을 내렸습니다. 국내제품 허가가 취소된 이후 절체절명의 위기를 맞이한 코오롱생명과학도 반전을 꿈꾸고 있는 것으로 보입니다. 하지만 식약처는 "미국 임상 재개는 국내 제품 허가 취소와 아무 상관 없다"고 단언하고 있습니다. 코오롱생명과학이 꿈꾸는 반전은 진짜 반전으로 이어질 수 있을까요?
-
-

이지윤 기자 easynews@kbs.co.kr
이지윤 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0














이 기사에 대한 의견을 남겨주세요.