식약처 “코로나 19 치료제 13건, 백신 2건 임상시험 승인”
입력 2020.06.26 (15:00)
수정 2020.06.26 (15:09)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.
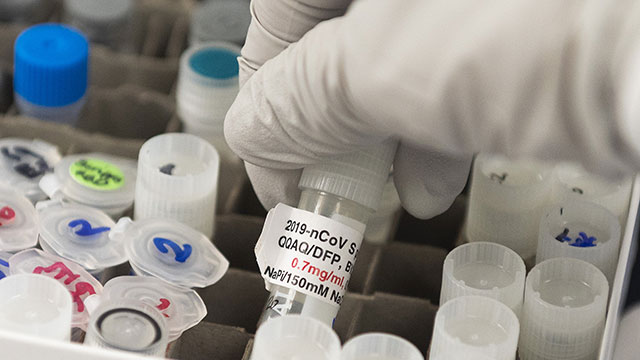
식품의약품안전처가 현재 국내에서 코로나 19 치료제와 백신 15건에 대한 임상시험이 승인됐다고 밝혔습니다.
식약처는 오늘(26일) 오후 열린 정례브리핑에서 국내외에서 개발되고 있는 치료제와 백신 등의 개발 진행 상황을 설명했습니다.
현재 국내에선 치료제 13건과 백신 2건의 임상시험이 승인됐고, 개발 단계별로 보면 3상 임상시험이 2건, 2상 임상시험이 4건, 연구자 임상시험이 7건입니다. 이 가운데 우리나라에서 개발한 치료제로는 2상 시험 중인 클레부딘, 피라맥스, EC-18, 나파모스타트가 있다고 밝혔습니다.
백신 임상시험 2건은 모두 초기 단계로 이 가운데 우리나라에서 개발한 백신은 GX-19입니다.
현재 국내외에서 코로나 19 치료제로 사용되고 있는 '덱사메타손'에 대해서는, 급성호흡기증후군과 같은 중증 환자에 한정해 의사가 환자 상태를 관찰하면서 투여하는 게 적절할 것으로 보인다고 설명했습니다. 식약처는 국내 수급은 원활하며, 정제 또는 주사제 14개 품목이 생산되고 있다고 밝혔습니다.
국제보건기구(WHO)와 미국 국립보건원(NIH)이 임상시험 자료 분석 결과 치료적 유익성이 없다고 판단한 '히드록시클로로퀸'에 대해서는, 국내 임상시험도 종료됐다고 설명했습니다.
식약처는 코로나 19 치료제와 백신의 사용, 개발 동향을 관찰해 품목허가와 공급에 필요한 사항을 지원해 나가겠다고 밝혔습니다.
[사진 출처 : AFP=연합뉴스]
 ▶ ‘ 코로나19 현황과 대응’ 최신 기사 보기
▶ ‘ 코로나19 현황과 대응’ 최신 기사 보기http://news.kbs.co.kr/news/listIssue.html?icd=19588
식약처는 오늘(26일) 오후 열린 정례브리핑에서 국내외에서 개발되고 있는 치료제와 백신 등의 개발 진행 상황을 설명했습니다.
현재 국내에선 치료제 13건과 백신 2건의 임상시험이 승인됐고, 개발 단계별로 보면 3상 임상시험이 2건, 2상 임상시험이 4건, 연구자 임상시험이 7건입니다. 이 가운데 우리나라에서 개발한 치료제로는 2상 시험 중인 클레부딘, 피라맥스, EC-18, 나파모스타트가 있다고 밝혔습니다.
백신 임상시험 2건은 모두 초기 단계로 이 가운데 우리나라에서 개발한 백신은 GX-19입니다.
현재 국내외에서 코로나 19 치료제로 사용되고 있는 '덱사메타손'에 대해서는, 급성호흡기증후군과 같은 중증 환자에 한정해 의사가 환자 상태를 관찰하면서 투여하는 게 적절할 것으로 보인다고 설명했습니다. 식약처는 국내 수급은 원활하며, 정제 또는 주사제 14개 품목이 생산되고 있다고 밝혔습니다.
국제보건기구(WHO)와 미국 국립보건원(NIH)이 임상시험 자료 분석 결과 치료적 유익성이 없다고 판단한 '히드록시클로로퀸'에 대해서는, 국내 임상시험도 종료됐다고 설명했습니다.
식약처는 코로나 19 치료제와 백신의 사용, 개발 동향을 관찰해 품목허가와 공급에 필요한 사항을 지원해 나가겠다고 밝혔습니다.
[사진 출처 : AFP=연합뉴스]

■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- 식약처 “코로나 19 치료제 13건, 백신 2건 임상시험 승인”
-
- 입력 2020-06-26 15:00:47
- 수정2020-06-26 15:09:48

식품의약품안전처가 현재 국내에서 코로나 19 치료제와 백신 15건에 대한 임상시험이 승인됐다고 밝혔습니다.
식약처는 오늘(26일) 오후 열린 정례브리핑에서 국내외에서 개발되고 있는 치료제와 백신 등의 개발 진행 상황을 설명했습니다.
현재 국내에선 치료제 13건과 백신 2건의 임상시험이 승인됐고, 개발 단계별로 보면 3상 임상시험이 2건, 2상 임상시험이 4건, 연구자 임상시험이 7건입니다. 이 가운데 우리나라에서 개발한 치료제로는 2상 시험 중인 클레부딘, 피라맥스, EC-18, 나파모스타트가 있다고 밝혔습니다.
백신 임상시험 2건은 모두 초기 단계로 이 가운데 우리나라에서 개발한 백신은 GX-19입니다.
현재 국내외에서 코로나 19 치료제로 사용되고 있는 '덱사메타손'에 대해서는, 급성호흡기증후군과 같은 중증 환자에 한정해 의사가 환자 상태를 관찰하면서 투여하는 게 적절할 것으로 보인다고 설명했습니다. 식약처는 국내 수급은 원활하며, 정제 또는 주사제 14개 품목이 생산되고 있다고 밝혔습니다.
국제보건기구(WHO)와 미국 국립보건원(NIH)이 임상시험 자료 분석 결과 치료적 유익성이 없다고 판단한 '히드록시클로로퀸'에 대해서는, 국내 임상시험도 종료됐다고 설명했습니다.
식약처는 코로나 19 치료제와 백신의 사용, 개발 동향을 관찰해 품목허가와 공급에 필요한 사항을 지원해 나가겠다고 밝혔습니다.
[사진 출처 : AFP=연합뉴스]
 ▶ ‘ 코로나19 현황과 대응’ 최신 기사 보기
▶ ‘ 코로나19 현황과 대응’ 최신 기사 보기http://news.kbs.co.kr/news/listIssue.html?icd=19588
식약처는 오늘(26일) 오후 열린 정례브리핑에서 국내외에서 개발되고 있는 치료제와 백신 등의 개발 진행 상황을 설명했습니다.
현재 국내에선 치료제 13건과 백신 2건의 임상시험이 승인됐고, 개발 단계별로 보면 3상 임상시험이 2건, 2상 임상시험이 4건, 연구자 임상시험이 7건입니다. 이 가운데 우리나라에서 개발한 치료제로는 2상 시험 중인 클레부딘, 피라맥스, EC-18, 나파모스타트가 있다고 밝혔습니다.
백신 임상시험 2건은 모두 초기 단계로 이 가운데 우리나라에서 개발한 백신은 GX-19입니다.
현재 국내외에서 코로나 19 치료제로 사용되고 있는 '덱사메타손'에 대해서는, 급성호흡기증후군과 같은 중증 환자에 한정해 의사가 환자 상태를 관찰하면서 투여하는 게 적절할 것으로 보인다고 설명했습니다. 식약처는 국내 수급은 원활하며, 정제 또는 주사제 14개 품목이 생산되고 있다고 밝혔습니다.
국제보건기구(WHO)와 미국 국립보건원(NIH)이 임상시험 자료 분석 결과 치료적 유익성이 없다고 판단한 '히드록시클로로퀸'에 대해서는, 국내 임상시험도 종료됐다고 설명했습니다.
식약처는 코로나 19 치료제와 백신의 사용, 개발 동향을 관찰해 품목허가와 공급에 필요한 사항을 지원해 나가겠다고 밝혔습니다.
[사진 출처 : AFP=연합뉴스]
 ▶ ‘ 코로나19 현황과 대응’ 최신 기사 보기
▶ ‘ 코로나19 현황과 대응’ 최신 기사 보기-
-

우한솔 기자 pine@kbs.co.kr
우한솔 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0
이슈
코로나19


















이 기사에 대한 의견을 남겨주세요.