“아스트라제네카, 미국에 코로나19 백신 정식승인 요청 검토”
입력 2021.05.08 (10:13)
수정 2021.05.08 (15:13)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.
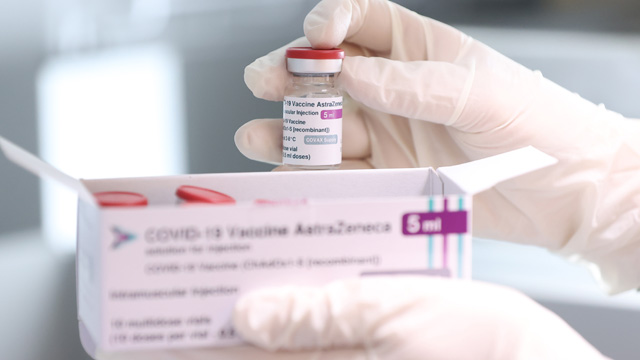
다국적 제약사 아스트라제네카가 미국 식품의약국(FDA)에 코로나19 백신에 대한 정식 승인 요청을 검토하고 있는 것으로 알려졌습니다.
미 월스트리트저널(WSJ)은 현지시간 어제(7일) 아스트라제네카가 긴급사용 승인 단계를 생략하고 곧바로 정식 승인을 요청하는 방안을 검토 중이라고 보도했습니다.
공중보건 위기가 닥쳤을 때 의약품 활용도를 높이기 위해 내리는 임시 조치인 긴급사용 승인과 달리, 정식 승인 절차는 요건이 엄격해 수개월이 걸리는 것으로 알려져있습니다.
아스트라제네카가 미 FDA에 정식 승인 신청을 검토하는 것은 긴급사용 승인 신청이 지연되고 있기 때문이라고 WSJ은 전했습니다.
앞서 아스트라제네카는 지난달 중순까지 긴급사용 승인을 신청하겠다고 공표했지만, 실제 접종 결과에 대한 데이터를 정리하는 데 시간이 걸리면서 어려움을 겪고 있는 것으로 알려졌습니다.
아스트라제네카 대변인은 지난달 30일 FDA에 방대한 자료를 제출해왔다면서 “자료에는 최근까지 진행한 임상시험 결과뿐만 아니라 실제 접종 데이터도 포함된다”고 설명했습니다.
WSJ은 다만 미국은 이미 긴급사용 승인을 받은 화이자와 모더나, 얀센 백신만으로도 접종계획을 충분히 진행할 수 있는 상황이기 때문에, 미 FDA가 아스트라제네카 코로나19 백신을 정식으로 승인할지는 불확실한 상황이라고 전했습니다.
또 아스트라제네카 백신 접종자 가운데 혈소판 감소를 동반하는 특이 혈전을 보인 사례가 있었다는 점도 정식 승인에 걸림돌이 될 것이라고 WSJ은 덧붙였습니다.
[사진 출처 : 연합뉴스]

미 월스트리트저널(WSJ)은 현지시간 어제(7일) 아스트라제네카가 긴급사용 승인 단계를 생략하고 곧바로 정식 승인을 요청하는 방안을 검토 중이라고 보도했습니다.
공중보건 위기가 닥쳤을 때 의약품 활용도를 높이기 위해 내리는 임시 조치인 긴급사용 승인과 달리, 정식 승인 절차는 요건이 엄격해 수개월이 걸리는 것으로 알려져있습니다.
아스트라제네카가 미 FDA에 정식 승인 신청을 검토하는 것은 긴급사용 승인 신청이 지연되고 있기 때문이라고 WSJ은 전했습니다.
앞서 아스트라제네카는 지난달 중순까지 긴급사용 승인을 신청하겠다고 공표했지만, 실제 접종 결과에 대한 데이터를 정리하는 데 시간이 걸리면서 어려움을 겪고 있는 것으로 알려졌습니다.
아스트라제네카 대변인은 지난달 30일 FDA에 방대한 자료를 제출해왔다면서 “자료에는 최근까지 진행한 임상시험 결과뿐만 아니라 실제 접종 데이터도 포함된다”고 설명했습니다.
WSJ은 다만 미국은 이미 긴급사용 승인을 받은 화이자와 모더나, 얀센 백신만으로도 접종계획을 충분히 진행할 수 있는 상황이기 때문에, 미 FDA가 아스트라제네카 코로나19 백신을 정식으로 승인할지는 불확실한 상황이라고 전했습니다.
또 아스트라제네카 백신 접종자 가운데 혈소판 감소를 동반하는 특이 혈전을 보인 사례가 있었다는 점도 정식 승인에 걸림돌이 될 것이라고 WSJ은 덧붙였습니다.
[사진 출처 : 연합뉴스]

■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- “아스트라제네카, 미국에 코로나19 백신 정식승인 요청 검토”
-
- 입력 2021-05-08 10:13:47
- 수정2021-05-08 15:13:10

다국적 제약사 아스트라제네카가 미국 식품의약국(FDA)에 코로나19 백신에 대한 정식 승인 요청을 검토하고 있는 것으로 알려졌습니다.
미 월스트리트저널(WSJ)은 현지시간 어제(7일) 아스트라제네카가 긴급사용 승인 단계를 생략하고 곧바로 정식 승인을 요청하는 방안을 검토 중이라고 보도했습니다.
공중보건 위기가 닥쳤을 때 의약품 활용도를 높이기 위해 내리는 임시 조치인 긴급사용 승인과 달리, 정식 승인 절차는 요건이 엄격해 수개월이 걸리는 것으로 알려져있습니다.
아스트라제네카가 미 FDA에 정식 승인 신청을 검토하는 것은 긴급사용 승인 신청이 지연되고 있기 때문이라고 WSJ은 전했습니다.
앞서 아스트라제네카는 지난달 중순까지 긴급사용 승인을 신청하겠다고 공표했지만, 실제 접종 결과에 대한 데이터를 정리하는 데 시간이 걸리면서 어려움을 겪고 있는 것으로 알려졌습니다.
아스트라제네카 대변인은 지난달 30일 FDA에 방대한 자료를 제출해왔다면서 “자료에는 최근까지 진행한 임상시험 결과뿐만 아니라 실제 접종 데이터도 포함된다”고 설명했습니다.
WSJ은 다만 미국은 이미 긴급사용 승인을 받은 화이자와 모더나, 얀센 백신만으로도 접종계획을 충분히 진행할 수 있는 상황이기 때문에, 미 FDA가 아스트라제네카 코로나19 백신을 정식으로 승인할지는 불확실한 상황이라고 전했습니다.
또 아스트라제네카 백신 접종자 가운데 혈소판 감소를 동반하는 특이 혈전을 보인 사례가 있었다는 점도 정식 승인에 걸림돌이 될 것이라고 WSJ은 덧붙였습니다.
[사진 출처 : 연합뉴스]

미 월스트리트저널(WSJ)은 현지시간 어제(7일) 아스트라제네카가 긴급사용 승인 단계를 생략하고 곧바로 정식 승인을 요청하는 방안을 검토 중이라고 보도했습니다.
공중보건 위기가 닥쳤을 때 의약품 활용도를 높이기 위해 내리는 임시 조치인 긴급사용 승인과 달리, 정식 승인 절차는 요건이 엄격해 수개월이 걸리는 것으로 알려져있습니다.
아스트라제네카가 미 FDA에 정식 승인 신청을 검토하는 것은 긴급사용 승인 신청이 지연되고 있기 때문이라고 WSJ은 전했습니다.
앞서 아스트라제네카는 지난달 중순까지 긴급사용 승인을 신청하겠다고 공표했지만, 실제 접종 결과에 대한 데이터를 정리하는 데 시간이 걸리면서 어려움을 겪고 있는 것으로 알려졌습니다.
아스트라제네카 대변인은 지난달 30일 FDA에 방대한 자료를 제출해왔다면서 “자료에는 최근까지 진행한 임상시험 결과뿐만 아니라 실제 접종 데이터도 포함된다”고 설명했습니다.
WSJ은 다만 미국은 이미 긴급사용 승인을 받은 화이자와 모더나, 얀센 백신만으로도 접종계획을 충분히 진행할 수 있는 상황이기 때문에, 미 FDA가 아스트라제네카 코로나19 백신을 정식으로 승인할지는 불확실한 상황이라고 전했습니다.
또 아스트라제네카 백신 접종자 가운데 혈소판 감소를 동반하는 특이 혈전을 보인 사례가 있었다는 점도 정식 승인에 걸림돌이 될 것이라고 WSJ은 덧붙였습니다.
[사진 출처 : 연합뉴스]

-
-

이중근 기자 news24@kbs.co.kr
이중근 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0
이슈
코로나19













![[단독] 국가안보실장 “한러, 서로 ‘레버리지’ 있어…<br>우크라 전쟁 끝나면 관계 복원”](/data/news/2024/04/27/20240427_a9hCZE.jpg)




이 기사에 대한 의견을 남겨주세요.