美 FDA “모더나 부스터샷에 회의적”
입력 2021.10.13 (09:10)
수정 2021.10.13 (09:25)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.
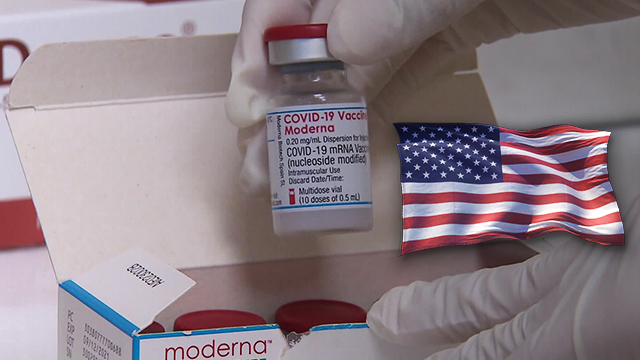
미국 식품의약국, FDA가 제약업체 모더나의 코로나19 백신이 부스터샷을 위한 기준에 모두 부합하는 것은 아니라는 입장을 밝혔습니다.
로이터 통신에 따르면 FDA는 현지 시간 12일 공개한 문건에서 모더나 백신의 부스터샷이 필요하지 않을 수 있는 이유로 애초 두 차례 접종 뒤 예방 효과가 강하게 지속된다는 점을 들었습니다.
FDA는 부스터샷 때문에 항체가 늘어날 수 있지만 접종 전후의 항체 수준차가 충분히 크지 않고, 특히 많은 항체를 보유한 접종자들의 경우에 그런 현상이 나타난다고 지적했습니다.
이번 문건은 FDA의 외부 자문기구인 백신·생물의약품자문위원회가 오는 14∼15일 모더나와 얀센 백신의 부스터샷이 필요한지 논의하기로 한 가운데 공개됐습니다.
일반적으로 FDA는 자문위의 권고를 대체로 받아들이지만 수용이 의무는 아닙니다.
미국 질병통제예방센터 CDC는 FDA가 모더나 백신의 부스터샷을 승인하면 접종 대상을 누구로 권고할지를 두고 다음 주 회의를 열기로 했습니다.
앞서 모더나는 애초 4주 정도 간격으로 두 차례 접종되는 자사 백신을 투여량을 절반 줄여 65세 이상 고령자와 고위험군에 한 차례 더 접종하는 방식으로 부스터샷을 시행하겠다고 승인을 요청했습니다.
로이터 통신에 따르면 FDA는 현지 시간 12일 공개한 문건에서 모더나 백신의 부스터샷이 필요하지 않을 수 있는 이유로 애초 두 차례 접종 뒤 예방 효과가 강하게 지속된다는 점을 들었습니다.
FDA는 부스터샷 때문에 항체가 늘어날 수 있지만 접종 전후의 항체 수준차가 충분히 크지 않고, 특히 많은 항체를 보유한 접종자들의 경우에 그런 현상이 나타난다고 지적했습니다.
이번 문건은 FDA의 외부 자문기구인 백신·생물의약품자문위원회가 오는 14∼15일 모더나와 얀센 백신의 부스터샷이 필요한지 논의하기로 한 가운데 공개됐습니다.
일반적으로 FDA는 자문위의 권고를 대체로 받아들이지만 수용이 의무는 아닙니다.
미국 질병통제예방센터 CDC는 FDA가 모더나 백신의 부스터샷을 승인하면 접종 대상을 누구로 권고할지를 두고 다음 주 회의를 열기로 했습니다.
앞서 모더나는 애초 4주 정도 간격으로 두 차례 접종되는 자사 백신을 투여량을 절반 줄여 65세 이상 고령자와 고위험군에 한 차례 더 접종하는 방식으로 부스터샷을 시행하겠다고 승인을 요청했습니다.
■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- 美 FDA “모더나 부스터샷에 회의적”
-
- 입력 2021-10-13 09:10:56
- 수정2021-10-13 09:25:03


미국 식품의약국, FDA가 제약업체 모더나의 코로나19 백신이 부스터샷을 위한 기준에 모두 부합하는 것은 아니라는 입장을 밝혔습니다.
로이터 통신에 따르면 FDA는 현지 시간 12일 공개한 문건에서 모더나 백신의 부스터샷이 필요하지 않을 수 있는 이유로 애초 두 차례 접종 뒤 예방 효과가 강하게 지속된다는 점을 들었습니다.
FDA는 부스터샷 때문에 항체가 늘어날 수 있지만 접종 전후의 항체 수준차가 충분히 크지 않고, 특히 많은 항체를 보유한 접종자들의 경우에 그런 현상이 나타난다고 지적했습니다.
이번 문건은 FDA의 외부 자문기구인 백신·생물의약품자문위원회가 오는 14∼15일 모더나와 얀센 백신의 부스터샷이 필요한지 논의하기로 한 가운데 공개됐습니다.
일반적으로 FDA는 자문위의 권고를 대체로 받아들이지만 수용이 의무는 아닙니다.
미국 질병통제예방센터 CDC는 FDA가 모더나 백신의 부스터샷을 승인하면 접종 대상을 누구로 권고할지를 두고 다음 주 회의를 열기로 했습니다.
앞서 모더나는 애초 4주 정도 간격으로 두 차례 접종되는 자사 백신을 투여량을 절반 줄여 65세 이상 고령자와 고위험군에 한 차례 더 접종하는 방식으로 부스터샷을 시행하겠다고 승인을 요청했습니다.
로이터 통신에 따르면 FDA는 현지 시간 12일 공개한 문건에서 모더나 백신의 부스터샷이 필요하지 않을 수 있는 이유로 애초 두 차례 접종 뒤 예방 효과가 강하게 지속된다는 점을 들었습니다.
FDA는 부스터샷 때문에 항체가 늘어날 수 있지만 접종 전후의 항체 수준차가 충분히 크지 않고, 특히 많은 항체를 보유한 접종자들의 경우에 그런 현상이 나타난다고 지적했습니다.
이번 문건은 FDA의 외부 자문기구인 백신·생물의약품자문위원회가 오는 14∼15일 모더나와 얀센 백신의 부스터샷이 필요한지 논의하기로 한 가운데 공개됐습니다.
일반적으로 FDA는 자문위의 권고를 대체로 받아들이지만 수용이 의무는 아닙니다.
미국 질병통제예방센터 CDC는 FDA가 모더나 백신의 부스터샷을 승인하면 접종 대상을 누구로 권고할지를 두고 다음 주 회의를 열기로 했습니다.
앞서 모더나는 애초 4주 정도 간격으로 두 차례 접종되는 자사 백신을 투여량을 절반 줄여 65세 이상 고령자와 고위험군에 한 차례 더 접종하는 방식으로 부스터샷을 시행하겠다고 승인을 요청했습니다.
-
-

심연희 기자 simony@kbs.co.kr
심연희 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0
이슈
코로나19


















이 기사에 대한 의견을 남겨주세요.