식약처, 한미약품 폐암신약 ‘제한적 사용’ 허용
입력 2016.10.04 (12:09)
수정 2016.10.04 (12:16)
읽어주기 기능은 크롬기반의
브라우저에서만 사용하실 수 있습니다.
<앵커 멘트>
한미약품의 신약 '올리타'에 대해 식품의약품안전처가 판매허가를 유지한 채 제한적 사용을 허용했습니다.
다만, 사용환자 대상 전수 모니터링 등 부작용에 대한 감시는 계속하기로 했습니다.
김기화 기자의 보도입니다.
<리포트>
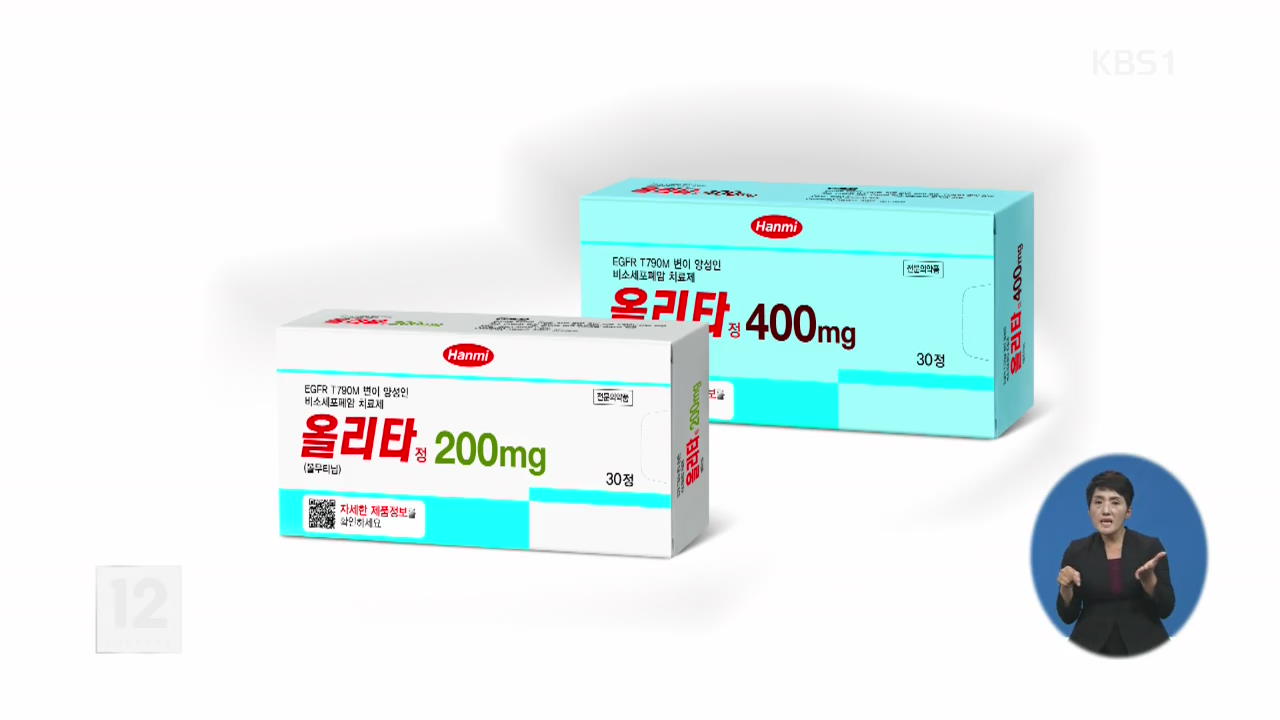
환자가 부작용으로 숨진 사실이 드러나 문제가 된 한미약품의 신약 '올리타'.
식품의약품안전처는 말기암 환자 치료를 고려해 제한적 사용을 허용하기로 결정했습니다.
다만 의사 판단하에 부작용발생 가능성 설명 후 환자 동의를 받아서 사용을 하는, 조건부 승인입니다.
또 사용환자 대상 전수 모니터링도 실시하기로 했습니다.
식약처는 안정성 정보와 중앙약사심의위원회의 자문결과, 대체 치료방법이 없는 환자에게 치료기회 제공 등을 종합적으로 고려한 결정이라고 밝혔습니다.
올리타에서 중증피부이상반응이 나타났지만, 기존치료에 실패한 말기 폐암환자에서 올리타의 유익성이 위험성보다 높다고 판단했다는 겁니다.
또, 투약을 중단할 경우 급격한 증세 악화 우려도 고려한 것으로 알려졌습니다.
식약처는 이에 따라 기존에 이 약을 먹던 환자에게 지속적으로 제공할 필요가 있고, 다른 항암제가 더 이상 듣지 않는 환자에게도 치료기회를 제공해야 한다고 권고했습니다.
말기 폐암 환자들을 위한 한미약품의 '올리타'는 2상 임상 시험 단계를 거쳐 지난 5월 식약처의 조건부 승인을 받았습니다.
허가 받기 한달전인 올 4월, 환자에게 중증피부질환이 나타나 사망했지만, 당시 식약처는 올리타와의 연관성이 명확하지 않다며 조건부 승인한바 있습니다.
KBS 뉴스 김기화입니다.
한미약품의 신약 '올리타'에 대해 식품의약품안전처가 판매허가를 유지한 채 제한적 사용을 허용했습니다.
다만, 사용환자 대상 전수 모니터링 등 부작용에 대한 감시는 계속하기로 했습니다.
김기화 기자의 보도입니다.
<리포트>
환자가 부작용으로 숨진 사실이 드러나 문제가 된 한미약품의 신약 '올리타'.
식품의약품안전처는 말기암 환자 치료를 고려해 제한적 사용을 허용하기로 결정했습니다.
다만 의사 판단하에 부작용발생 가능성 설명 후 환자 동의를 받아서 사용을 하는, 조건부 승인입니다.
또 사용환자 대상 전수 모니터링도 실시하기로 했습니다.
식약처는 안정성 정보와 중앙약사심의위원회의 자문결과, 대체 치료방법이 없는 환자에게 치료기회 제공 등을 종합적으로 고려한 결정이라고 밝혔습니다.
올리타에서 중증피부이상반응이 나타났지만, 기존치료에 실패한 말기 폐암환자에서 올리타의 유익성이 위험성보다 높다고 판단했다는 겁니다.
또, 투약을 중단할 경우 급격한 증세 악화 우려도 고려한 것으로 알려졌습니다.
식약처는 이에 따라 기존에 이 약을 먹던 환자에게 지속적으로 제공할 필요가 있고, 다른 항암제가 더 이상 듣지 않는 환자에게도 치료기회를 제공해야 한다고 권고했습니다.
말기 폐암 환자들을 위한 한미약품의 '올리타'는 2상 임상 시험 단계를 거쳐 지난 5월 식약처의 조건부 승인을 받았습니다.
허가 받기 한달전인 올 4월, 환자에게 중증피부질환이 나타나 사망했지만, 당시 식약처는 올리타와의 연관성이 명확하지 않다며 조건부 승인한바 있습니다.
KBS 뉴스 김기화입니다.
■ 제보하기
▷ 카카오톡 : 'KBS제보' 검색, 채널 추가
▷ 전화 : 02-781-1234, 4444
▷ 이메일 : kbs1234@kbs.co.kr
▷ 유튜브, 네이버, 카카오에서도 KBS뉴스를 구독해주세요!
- 식약처, 한미약품 폐암신약 ‘제한적 사용’ 허용
-
- 입력 2016-10-04 12:10:36
- 수정2016-10-04 12:16:48
<앵커 멘트>
한미약품의 신약 '올리타'에 대해 식품의약품안전처가 판매허가를 유지한 채 제한적 사용을 허용했습니다.
다만, 사용환자 대상 전수 모니터링 등 부작용에 대한 감시는 계속하기로 했습니다.
김기화 기자의 보도입니다.
<리포트>
환자가 부작용으로 숨진 사실이 드러나 문제가 된 한미약품의 신약 '올리타'.
식품의약품안전처는 말기암 환자 치료를 고려해 제한적 사용을 허용하기로 결정했습니다.
다만 의사 판단하에 부작용발생 가능성 설명 후 환자 동의를 받아서 사용을 하는, 조건부 승인입니다.
또 사용환자 대상 전수 모니터링도 실시하기로 했습니다.
식약처는 안정성 정보와 중앙약사심의위원회의 자문결과, 대체 치료방법이 없는 환자에게 치료기회 제공 등을 종합적으로 고려한 결정이라고 밝혔습니다.
올리타에서 중증피부이상반응이 나타났지만, 기존치료에 실패한 말기 폐암환자에서 올리타의 유익성이 위험성보다 높다고 판단했다는 겁니다.
또, 투약을 중단할 경우 급격한 증세 악화 우려도 고려한 것으로 알려졌습니다.
식약처는 이에 따라 기존에 이 약을 먹던 환자에게 지속적으로 제공할 필요가 있고, 다른 항암제가 더 이상 듣지 않는 환자에게도 치료기회를 제공해야 한다고 권고했습니다.
말기 폐암 환자들을 위한 한미약품의 '올리타'는 2상 임상 시험 단계를 거쳐 지난 5월 식약처의 조건부 승인을 받았습니다.
허가 받기 한달전인 올 4월, 환자에게 중증피부질환이 나타나 사망했지만, 당시 식약처는 올리타와의 연관성이 명확하지 않다며 조건부 승인한바 있습니다.
KBS 뉴스 김기화입니다.
한미약품의 신약 '올리타'에 대해 식품의약품안전처가 판매허가를 유지한 채 제한적 사용을 허용했습니다.
다만, 사용환자 대상 전수 모니터링 등 부작용에 대한 감시는 계속하기로 했습니다.
김기화 기자의 보도입니다.
<리포트>
환자가 부작용으로 숨진 사실이 드러나 문제가 된 한미약품의 신약 '올리타'.
식품의약품안전처는 말기암 환자 치료를 고려해 제한적 사용을 허용하기로 결정했습니다.
다만 의사 판단하에 부작용발생 가능성 설명 후 환자 동의를 받아서 사용을 하는, 조건부 승인입니다.
또 사용환자 대상 전수 모니터링도 실시하기로 했습니다.
식약처는 안정성 정보와 중앙약사심의위원회의 자문결과, 대체 치료방법이 없는 환자에게 치료기회 제공 등을 종합적으로 고려한 결정이라고 밝혔습니다.
올리타에서 중증피부이상반응이 나타났지만, 기존치료에 실패한 말기 폐암환자에서 올리타의 유익성이 위험성보다 높다고 판단했다는 겁니다.
또, 투약을 중단할 경우 급격한 증세 악화 우려도 고려한 것으로 알려졌습니다.
식약처는 이에 따라 기존에 이 약을 먹던 환자에게 지속적으로 제공할 필요가 있고, 다른 항암제가 더 이상 듣지 않는 환자에게도 치료기회를 제공해야 한다고 권고했습니다.
말기 폐암 환자들을 위한 한미약품의 '올리타'는 2상 임상 시험 단계를 거쳐 지난 5월 식약처의 조건부 승인을 받았습니다.
허가 받기 한달전인 올 4월, 환자에게 중증피부질환이 나타나 사망했지만, 당시 식약처는 올리타와의 연관성이 명확하지 않다며 조건부 승인한바 있습니다.
KBS 뉴스 김기화입니다.
-
-

김기화 기자 kimkoon@kbs.co.kr
김기화 기자의 기사 모음
-
이 기사가 좋으셨다면
-
좋아요
0
-
응원해요
0
-
후속 원해요
0














![[단독] ‘계엄의 밤’ 수사관 81명 대기했다…‘체포조’ 위해서였나](/data/news/2024/12/22/20241222_2B6xvY.jpg)


이 기사에 대한 의견을 남겨주세요.